Экзема: патология, лечение, помощь пациентам в кабинете косметолога
Истинная экзема — повсеместно встречающееся, чаще острое, реже хроническое рецидивирующее заболевание кожи, возникающее в любом возрасте, характеризующееся полиморфизмом морфологических элементов сыпи. Название данного дерматоза объясняется свойством экзематозных пузырьков быстро вскрываться, подобно пузырькам кипящей воды (по-гречески Ekzeo — вскипать). Важный признак острой экземы — наличие многочисленных сгруппированных и быстро вскрывающихся с образованием серозных «колодцев» мелких пузырьков, имеющих некоторое сходство с пузырьками на поверхности кипящей воды.
Этиология и патогенез заболевания
Этиологический и патогенетический аспекты развития экземы, освещённые в современных научных изданиях, носят весьма противоречивый характер. Патогенез экземы привлекал внимание многих исследователей. Они выдвигали различные теории ее происхождения и связывали возникновение экземы с преобладающими нарушениями в той или иной системе организма.
На современном этапе развития учения об экземе основное значение придают патогенетической роли различных иммунных сдвигов, изменениям состояния простагландинов и циклических нуклеотидов. При изучении иммунного статуса больных экземой были установлены значительные нарушения клеточного звена иммунитета и неспецифических факторов защиты, проявляющиеся в выраженной лимфоцитопении, снижении функциональной активности и содержания пула Т-лимфоцитов, резком подавлении функциональной активности Т-супрессоров и уменьшении количества Т-хелперов. Выявленные нарушения находились в прямой зависимости от продолжительности заболевания, выраженности клинических проявлений и изменялись с возрастом.
Значительную роль в патогенезе экземы играют изменения состояния простагландинов и циклических нуклеотидов, которые занимают центральное место во внутриклеточных регуляторных механизмах, опосредуют нейроэндокринную информацию, превращают ее в специфический ответ клетки и реализуют нормальные и патологические реакции организма.
Установленные биохимические и иммунные нарушения позволили разработать новую концепцию патогенеза экземы. У лиц, имеющих наследственную предрасположенность, подтверждаемую положительной ассоциацией антигенов системы гистосовместимости (В22 и Сw1), повышается синтез простагландина F2а, что вызывает усиленную стимуляцию синтеза циклического гуанозинмонофосфата, который активирует выработку гистамина, серотонина и других медиаторов аллергии, способствует развитию аллергических и воспалительных реакций, повышению проницаемости сосудов. Одновременно с увеличением образования простагландина F2а повышается синтез простагландина Е1, но его концентрация значительно снижена по отношению к увеличивающейся концентрации простагландина F201. Недостаток содержания простагландина Е1, нарушение его соотношения с содержанием простагландина F2а приводит к недостаточной стимуляции синтеза циклического аденозинмонофосфата, подавляющего формирование аллергических и воспалительных реакций, выработку медиаторов аллергии.
Таким образом, у больных экземой в результате повышения содержания F2а и нарушения соотношения ПГE1/ПГФ2а и цАМФ/цГМФ происходит преобладание простагландина F2а и циклического гуанозинмонофосфата, что является одной из причин развития заболевания.
В тромбоцитах периферической крови больных экземой установлено усиление синтеза и экскреции серотонина в кровяное русло. Реакция высвобождения тромбоцитов, в результате которой серотонин поступает в кровь, регулируется простагландинами. Простагландин Е1 ее подавляет, а простагландин F2а провоцирует.
Преобладание простагландина F2а обусловливает повышение содержания в крови серотонина, что усугубляет аллергические реакции. Гормон щитовидной железы тиреокальцитонин стимулирует активность аденилатциклазы — фермента, катализирующего синтез циклического аденозинмоно-фосфата из АТФ. Повышение содержания тиреокальцитонина у больных экземой, возможно, и есть проявление защитно-компенсаторных реакций организма.
Простагландины и циклические нуклеотиды являются одним из факторов многокомпонентной системы регуляции иммунного ответа. Повышение их синтеза приводит к изменениям иммунологической реактивности и вызывает глубокие иммунологические расстройства, проявляющиеся в подавлении клеточного иммунитета (снижение содержания Т-РОК, количественных и функциональных показателей Т-хелперов и Т-супрессоров, подавление супрессорной активности Т-лимфоцитов) и неспецифических факторов защиты (снижение количества спонтанных и комплементарных нейтрофилов, содержания цитоплазматических гранул нейтрофильных лейкоцитов, процента фагоцитоза, абсолютного фагоцитарного показателя и фагоцитарного числа). Изменения иммунного статуса способствуют повышению аллергической реактивности и наряду с простагландинами и циклическими нуклеотидами приводят к формированию экзематозного процесса. Степень выраженности установленных нарушений дисбаланса простагландинов, циклических нуклеотидов и иммунологической реактивности отражается на остроте клинических проявлений и течении процесса.
Одновременно с состоянием иммунной недостаточности у больных экземой констатируют функциональные изменения в деятельности ЦНС, преобладание активности безусловных рефлексов над активностью условных рефлексов, нарушения равновесия между деятельностью симпатических и парасимпатических отделов вегетативной нервной системы, изменения функционального состояния рецепторов кожи в виде диссоциации кожной чувствительности. Таким образом, угнетение иммунной реактивности у больных экземой развивается не изолированно, не только на основе генетической предрасположенности, но и в результате сложных нейроэндокринно-гуморальных сдвигов, изменяющих трофику тканей.
Безусловно, основным, но не единственным механизмом формирования экземы следует признать аллергические реакции 1-го типа. Какие бы типы аллергических реакций не принимали участие в формировании данного заболевания, ключевым звеном патогенеза экземы является выработка у этих больных противовоспалительных цитокинов и хемокинов, ответственных за формирование хронического аллергического воспаления. Это в первую очередь IL-4 и рецептор к IL-4, IL-5, IL-6, IL-10, IL -13, IL-18, ТGFb (трансформирующий фактор роста-бета), ТNFа (фактор некроза опухоли-альфа), GМ-CSF(грануляцитарно-макрофагальный колониестимулирующий фактор), IFNj (интерферон-гамма).
В современной литературе собрано большое количество наблюдений, указывающих на связь аллергических заболеваний у родителей или родственников больного с появлением каких-либо аллергических проявлений у детей. Если оба родителя ребенка страдают аллергическим заболеванием, то риск формирования экземы по разным данным составляет от 50% до 8о%, если наследственность отягощена по материнской линии, то риск развития аллергического заболевания составляет от 30% до 50%.
Ирландские ученые впервые идентифицировали ген, отвечающий за склонность к шелушению и сухости кожи, а также за предрасположенность к развитию экземы . Было установлено, что люди, в геноме которых содержится мутантный вариант гена, ответственного за синтез белка филаггрина (filaggrin), в больших количествах содержащегося в поверхностных слоях кожи, склонны к развитию экземы. Этот белок необходим для формирования защитного слоя поверхности кожи. У двух третей обследованных детей, страдающих экземой, была обнаружена как минимум одна мутация гена, кодирующего филаггрин. Кроме того, оказалось, что 9% европейцев страдают от сухости и шелушения кожи в результате нарушения функционирования этого гена.
Ученые медицинского факультета Университета Вашингтона в Сент-Луисе обнаружили ген, способный, по их мнению, вызвать экзему. Они изучали работу гена GRPR (gastrin-releasing peptide receptor — гастрин-высвобождающий пептидный рецептор). Называется он так из-за связи с рецептором в спинном мозге, передающим сигналы раздражения (боль и зуд) с кожи в головной мозг. Его стимулирование заставляло мышей активно чесаться. А блокирование GRPR приводило к тому, что мышки чесались меньше, чем контрольная группа..
Тайваньские исследователи, изучавшие влияние ингибитора сериновой протеазы Kazal типа 5 (SPINK5) и IL- 13 на формирование истинной экземы показали, что rs6892205 G аллель SPINK5 и rs20541 аллель IL13 были связаны с развитием истинной экземы.
Голландские ученые исследовали влияние полиморфизма генов, кодирующих интерлейкин (IL) -1 а, ИЛ-1 b, IL-8, IL-10 и фактора некроза опухоли ФНО а на экзематозное воспаление кожи. Результаты показали, что для всех полиморфизмов не было выявлено никаких различий между пациентами с экземой и контрольной группой. Однако, у пациентов, чья работа связана с влажными уборками и частым контактом с раздражающими средствами (санитарки, уборщицы), вариантов генотипов 308GA и -308АА TNFa больше, чем в контрольной группе. У пациентов с различными генотипами -308GA и -308АА TNFa распространенность атопического дерматита была выше (48% и 57%) по сравнению с пациентами с вариантным генотипом -308GG TNFa. Что касается IL1A -889, распространенность симптомов дерматита была ниже у пациентов с ТТ или СТ генотипом (32% и 36%) по сравнению с вариантным генотипом (54%, СС), что указывает на защитный эффект этих вариантов аллелей в приобретении экземы рук.
Таким образом, резюмируя представленные в статье материалы, можно отметить, что в настоящее время не существует единой общепризнанной теории возникновения истинной экземы. На развитие заболевания влияют множественные эндогенные (нейроаллергические, эндокринные, обменные и др.) средовые и наследственные факторы.
Классификация заболевания
Единой классификации экземы в настоящее время не существует. В зависимости от особенностей клинической картины выделяют следующие формы истинной экземы:
- Идиопатическая
- Дисгидротическая
- Пруригинозная
- Роговая (тилотическая)
По течению экзема подразделяется на острую (менее двух месяцев), подострую (не более шести месяцев) и хроническую (6 месяцев и более). В течении экземы четко выделяются следующие стадии: эритематозная, папуловезикулезная, мокнутия и лихенификации.
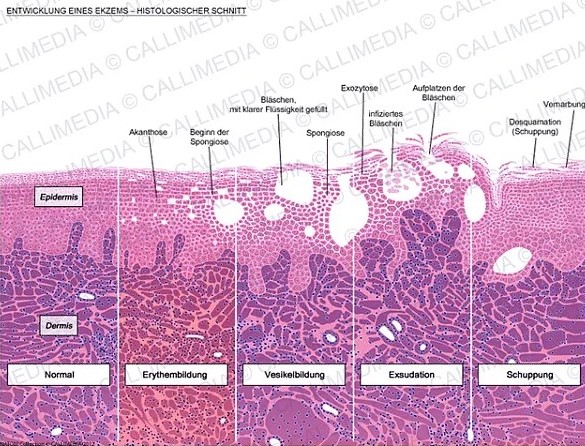
При эритематозной стадии экземы наблюдаются отек верхней половины дермы, ограниченные, в основном лимфоцитарные, инфильтраты, расширение сосудов сосочкового слоя дермы, набухание эндотелия, обеднение цитоплазмы рибосомами.
При папулезной или папуловезикулезной фазе кроме перечисленных гистологических признаков обнаруживают спонгиоз, акантоз с удлинением эпидермальных выростов, паракератоз и небольшую везикуляцию.
В фазе мокнутия отмечаются значительный спонгиоз с расширением межклеточных промежутков, разрушение десмосом и образование пузырей различных размеров. Пузырьки вскрываются и превращаются в так называемые «колодцы», из которых выделяется экссудат.
Сквамозная фаза характеризуется акантозом и паракератозом с отшелушиванием рогового слоя, незначительным отеком верхней части дермы.
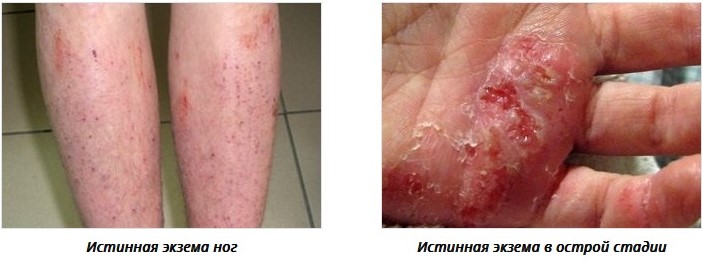
Истинная экзема (идиопатическая). Проявляется островоспалительной эритемой, отеком, на фоне которых формируются микровезикулы, а также экссудативные папулы. Микровезикулы быстро вскрываются, на их месте образуются точечные эрозии, так называемые серозные колодцы, из которых выделяется экссудат, образуя участки мокнутия с мацерированным и слущенным эпителием. Серозная жидкость постепенно подсыхает, формируя серовато-желтые корки.
Поражение кожи при истинной экземе обычно начинается с области кистей и/или стоп. Высыпания чаще симметричные, со склонностью к распространению на кожу предплечий, голеней и других участков кожного покрова. Очаги экземы имеют различные размеры с нечеткими границами. Характерно чередование пораженных участков кожи с непораженными ("архипелаг островов"). Пациентов беспокоит зуд различной степени интенсивности, что способствует развитию невротических расстройств, тревожности и нарушению сна. Экзематозный процесс может перейти в хроническое течение, клинически проявляясь очагами сухости, шелушения и образованием трещин. Нередко экзема осложняется присоединением инфекции с появлением пустул и гнойных корок.
Дисгидротическая экзема характеризуется появлением на боковых поверхностях пальцев кистей и стоп, на коже ладоней и подошв зудящих пузырьков, везикул с плотной покрышкой, иногда многокамерных величиной с булавочную головку. Располагаясь глубоко в эпидермисе пузырьки, просвечивают сквозь него, напоминая зерна сваренного риса. После вскрытия плотных покрышек пузырьков образуются эрозии с мокнутием и серозные корки, трещины и шелушение.
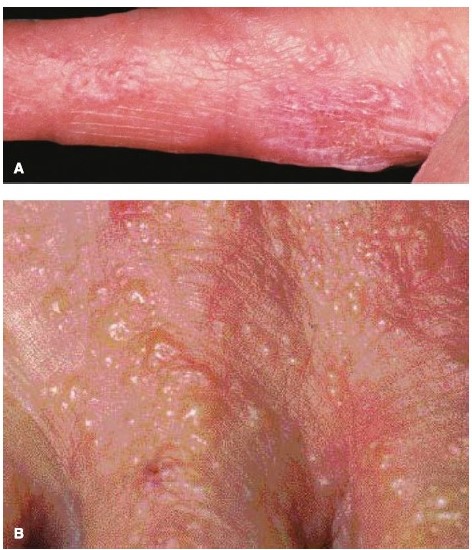
Рисунок 2. Сливающиеся везикулы, похожие на тапиоку, на боковых сторонах пальцев (А), перепонках между пальцами и тыльной стороне (B)
Пруригинозная экзема характеризуется мелкими, зудящими папуловезикулами на плотном основании, не вскрывающимися и не образующими корок. Излюбленная
локализация – лицо, разгибательные поверхности конечностей, локтевые и коленные сгибы, половые органы. Течение процесса хроническое с развитием на фоне расчесов,
инфильтрации, сухости и лихенификации.
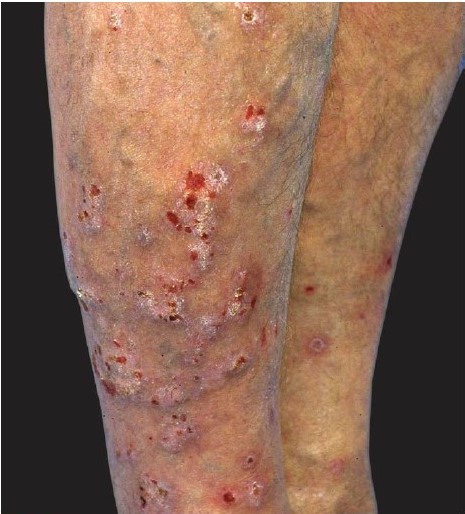
Рисунок 3. Множественные, твердые, раздраженные узелки, возникающие на участках хронически поврежденной кожи. Часто встречается у пациентов с атопией, но также и без нее. У этого 56-летнего пациента, сильный зуд потребовал многократной госпитализации.
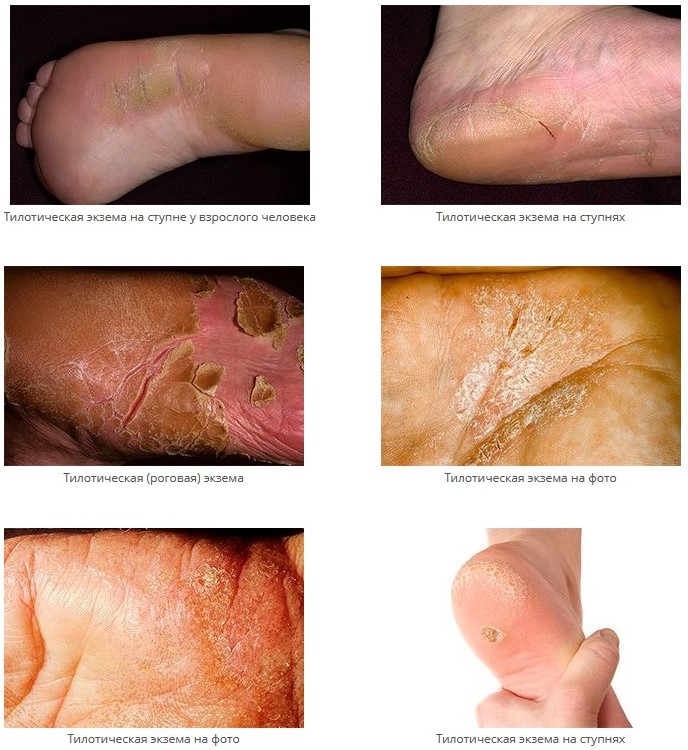
Роговая (тилотическая) экзема проявляется гиперкератозом ладоней и подошв с образованием грубых роговых и корковых наслоений, сухостью кожи, а также глубокими болезненными длительно не заживающими, нередко кровоточащими трещинами. Данное заболевание характеризуется поливалентной сенсибилизацией и аутосенсибилизацией, протекает на фоне нейроэндокринных сдвигов, сопровождается изменениями в центральной и вегетативной нервной системе, нарушениями обменных процессов и трофики тканей.
Поражение подошв и ладоней, как правило, симметричное, трещины формируются на фоне эритемы, шелушения, особенно на участках наибольшего давления и нагрузки, в том числе и на боковых поверхностях пальцев. Воспаление может быть выражено на ограниченном участке или занимать всю подошву и/или ладонь, боль в области трещин может быть более интенсивной, чем зуд. Тенденция к углублению трещин связана с возрастом пациента, длительностью болезни, холодным временем года и наличием фоновых заболеваний.
Диагностика заболевания
Диагноз экземы базируется на основании анализа жалоб, данных анамнеза, оценке
клинической картины заболевания.
При истинной экземе клиническая картина заболевания типична; в редких случаях истинную экзему приходится дифференцировать от атопического дерматита, токсидермий, пиодермий, аллергического контактного дерматита.
Экзему отличают от атопического дерматита по следующим параметрам: экссудация/сухость, отек/лихенизация, зуд слабый/сильный, реакция адренергическая/холинергическая, дермографизм красный/белый.
При контактном аллергическом дерматите и токсидермии эритема, отечность, папулезные и везикулезные элементы локализуются на участках, подвергающихся воздействию аллергена. Чаще это тыльная поверхность кистей, лицо, щеки, шея; реже нижние конечности, предплечья, плечи, хотя у некоторых больных имеется тенденция к распространению процесса и на закрытые участки кожного покрова. Повторные контакты с аллергенами способствуют трансформации аллергического дерматита в экзему. Основным отличием экземы от аллергического дерматита является его разрешение после устранения воздействия этиологического фактора, который удостоверяется положительными кожными пробами.
Дисгидротическую экзему следует дифференцировать от ладонно-подошвенного
псориаза, пустулезного бактерида Эндрюса, дерматомикозов, хронического акродерматита Аллопо, в исключительных случаях – от буллезного пемфигоида.
В отличии от ладонно-подошвенного псориаза клинической особенностью этой формы экземы являются крупные (5—6 мм) полостные элементы, похожие на пузыри. Они представляют собой слившиеся многокамерные спонгиотические везикулы. Гиперемия и отечность клинически не выражены. Все это объясняется толстым роговым слоем на ладонях и подошвах. Больных беспокоит интенсивный зуд, иногда «дергающие» боли. Полостные элементы сохраняются долго, самостоятельно не вскрываются (толстая покрышка).
Пустулезный бактерид ладоней и подошв Эндрюса начинается в центре ладоней и подошв, постепенно распространяясь вплоть до захвата боковых поверхностей. Первичными высыпаниями являются везикулы и пустулы. Нередко между пустулами отчетливо заметны точечные геморрагические пятнышки. Характерны интенсивный зуд и болезненность очагов. При затихании процесса очаги покрываются плотными чешуйками.
Гистологически в эпидермисе обнаруживаются глубокие пустулы, содержащие полинуклеарные лейкоциты и дегенерированные эпителиальные клетки. Вне пустул воспалительный инфильтрат отсутствует.
Санация очагов хронической инфекции, как правило, приводит к регрессу бактерида.
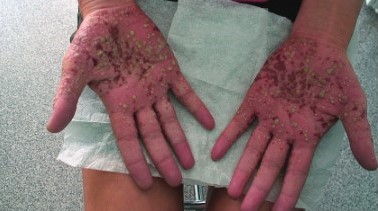
Рисунок 5. Пациентка К., 41 год. бактерид пустулезный Эндрюса с поражением ладоней
Хронический акродерматит Аллопо может начинаться в любом возрасте. Болеют чаще мужчины. Высыпания дебютируют на концевых фалангах пальцев рук, реже ног, постепенно распространяясь на другие участки кожи ладоней и подошв. В редких случаях процесс может принимать генерализованный характер. Ногтевые валики резко гиперемированы, отечны, инфильтрированы. Из-под них выделяется гной. В дальнейшем на коже всей поверхности ногтевой фаланги появляются пустулы или везикулы, постепенно полостные элементы могут подсыхать, покрываться корко-чешуйками.
Гистологическая картина идентична таковой при пустулезном псориазе. Субкорнеальные пустулы Когои стерильны. Дифференциальным признаком является возникновение атрофии кожи после разрешения очагов поражения.
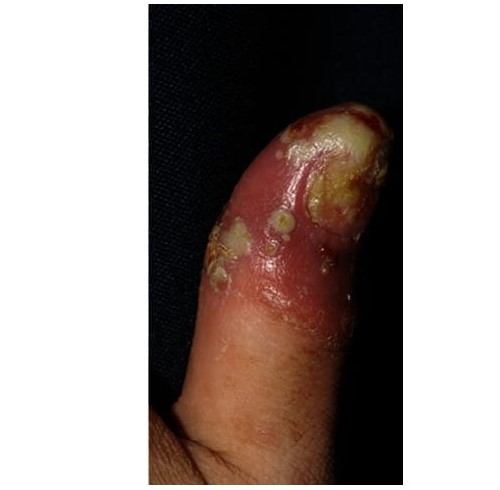
Рисунок 6. На этой фотографии показаны пустулезные поражения на кончике пальца у пациента со стойким акродерматитом Аллопо. © Springer Science+Business Media
Дифференциальный диагноз пруригинозной экземы проводят с чесоткой, детской
почесухой, стойкой папулезной крапивницей, герпетиформным дерматитом Дюринга.
Данные анамнеза и нахождение в соскобах рогового слоя чесоточного клеща позволяют поставить диагноз чесотки.
Герпетиформный дерматит (Дюринга) характеризуется наличием на коже полиморфной, нередко симметричной, склонной к группировке сыпи. Высыпания могут локализоваться на любом участке кожного покрова, за исключением ладоней и подошв. Диагностика в типичных случаях трудностей не представляет. Наличие склонной к группировке полиморфной сыпи и интенсивного зуда характерны для дерматита Дюринга.
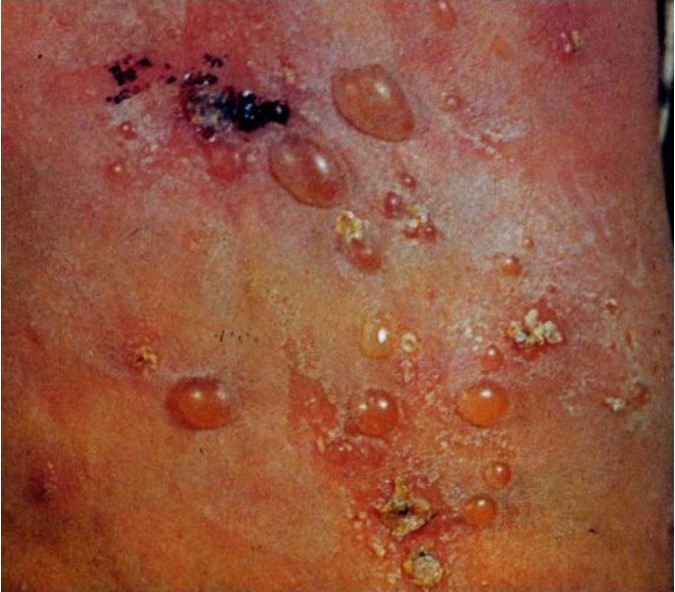
Рисунок 7. Герпетиформный дерматит (Дюринга)
Дифференциальный диагноз роговой (тилотической) экземы проводят с псориазом ладоней и подошв, дерматомикозом, кератодермией
В клинической картине дерматомикозов преобладает гиперкератоз, обильное диффузное шелушение ладоней и подошв. Трещины чаще всего наблюдаются по краю пяток. Часто наблюдается изменение формы и цвета ногтевых пластинок, краевой или тотальный онихолизис, в других случаях — гипертрофия ногтевых пластинок вплоть до онихогрифоза.
Для подтверждения диагноза микоза следует провести микроскопическое и культуральное исследование кожных чешуек.
ОБЩИЕ МЕТОДЫ ДИАГНОСТИКИ
- Рекомендуется при подозрении ассоциации экземы с паразитарными заболеваниями проведение:
микроскопическое исследование кала на яйца и личинки гельминтов.
определение антител классов A, M, G (IgM, IgA, IgG) к лямблиям в крови.
или
определение антител к аскаридам (Ascaris lumbricoides).
или
определение антител к возбудителю описторхоза (Opisthorchis felineus) в крови.
- Рекомендуется определение специфических антител к пищевым, бытовым антигенам, антигенам растительного, животного и химического происхождения при рецидивирующем, хроническом течении процесса.
- Рекомендуется микробиологическое (культуральное) исследование отделяемого высыпных элементов кожи на чувствительность к антибактериальным и противогрибковым препаратам при подозрении на присоединение вторичной инфекции.
- Рекомендуется патологоанатомического исследования биопсийного (операционного) материала кожи из очага поражения при необходимости проведения дифференциальной
диагностики с другими заболеваниями кожи.
При гистологическом исследовании биоптата кожи при экземе в остром процессе отмечают спонгиоз, большое количество мелких пузырьков в эпидермисе; внутриклеточный отек в клетках шиповатого слоя; в дерме – расширение сосудов поверхностной сосудистой сети, отек сосочков и лимфоидно-клеточная инфильтрация вокруг сосудов. Патогистологические изменения при хроническом процессе характеризуются наличием периваскулярного инфильтрата в дерме, состоящего из
лимфоцитов, фибробластов, гистиоцитов, эозинофилов. В эпидермисе – акантоз, гиперкератоз, паракератоз, незначительный отек.
Лечение заболевания
Для терапии пациентов с экземой используется системная и наружная лекарственнаятерапия, а также фототерапия
- Для уменьшения выраженности воспалительной реакции и зуда рекомендуются глюкокортикоиды: алклометазон 0,05%, метилпреднизолона ацепонат 0,1%, гидрокортизон, мометазон 0,1%, бетаметазон, клобетазол 0,05% крем.
- В случае риска вторичного инфицировании и/или в случае его развития рекомендуется обработка эрозий с применением антисептиков и дезинфецирующих препаратов
- При отсутствии вторичного инфицирования для наружной терапии рекомендуется назначение препаратов для лечения заболеваний кожи: пимекролимус 1%, такролимус 0,03%.
- Рекомендуется для наружной терапии с целью уменьшения экссудации и мокнутия назначения препаратов цинка.
- Для уменьшения интенсивности зуда рекомендуется назначение антигистаминных средств системного действия.
- Рекомендуется при выраженном зуде: хлоропирамин раствор для инъекций внутримышечно или клемастин раствор для инъекций внутримышечно или гидроксизин перорально.
- Рекомендуются при наличии выраженного воспаления или отсутствии тенденции к регрессу высыпаний глюкокортикостероиды для системного применения: бетаметазон 1,0 мл внутримышечно или преднизолон перорально или дексаметазон
- Рекомендуются при тилотической экземе в случаях выраженной инфильтрации, гиперкератоза и/или торпидности к проводимой терапии ретиноиды для лечения псориаза: ацитретин или фототерапия.
Экзема и инъекционная косметология
Истинная экзема является вариантом атопического дерматита (наряду с нейродермитом), имеет эндогенное происхождение. В связи с этим, мы можем рассмотреть и научные материалы, изучающие особенности инъекционной косметологии при атопическом дерматите, и экстраполировать их на случаи экземы.
БТА. Экзема/атопический дерматит не является противопоказанием для инъекций БТА, однако не стоит выполнять процедуру в период обострения и при наличии признаков вторичной инфекции в области введения препарата.
Согласно опубликованным данным пациенты с экземами могут получить не только косметологический, но и терапевтический эффект от инъекций БТА: в ряде исследований было показано, что инъекции БТА могут уменьшать интенсивность кожного зуда и выраженность воспаления кожи, так как БТА подавляет выброс ацетилхолина (главного медиатора кожного зуда) и снижает уровень экспрессии ИЛ-4 и некоторых других провоспалительных цитокинов. Можно предположить, что инъекции БТА для коррекции потоотделения (в область подмышек, стоп, ладоней) могут улучшать состояние тех больных экземой, у которых заболевание обостряется при повышенном потоотделении.
Филлеры на основе ГК. Формально экзема/ атопический дерматит не является противопоказанием для инъекций ГК, однако есть ряд нюансов, которые стоит учитывать. В литературе описано довольно много клинических случаев аллергических реакций на инъекционные препараты ГК, причем как реакций немедленного типа (IgE-опосредованные реакции), так и реакций замедленного типа (чаще всего в виде формирования гранулем в месте введения препарата).
На иммуногенность и аллергенность препаратов гк влияет множество факторов:
Источник ГК: получена ли она из животного материала (может быть потенциально аллергенным, поэтому в настоящее время почти не используется) или путем лабораторного синтеза (может содержать бактериальные антигены, стабилизаторы и другие химические вещества, используемые в производстве).
Размер молекул ГК: низкомолекулярная ГК обладает провоспалительным эффектом, высокомолекулярная ГК, напротив, противовоспалительным эффектом. Как правило, в препаратах используют оба вида ГК в различных соотношениях, и от этого зависят плотность и эластичность препарата.
Дополнительные компоненты филлеров: анестетики (лидокаин), влагоудерживатели (маннитол, декстран), консерванты, стабилизаторы.
Реакции немедленного типа, как правило, обусловлены не самой ГК, а именно дополнительными веществами, входящими в состав филлеров ГК, в частности лидокаином. Поэтому, врач, выполняющий инъекцию, должен тщательно собрать анамнез и убедиться, что у пациента ранее не было аллергических реакций ни на один из компонентов препарата, который ему будут вводить.
Мезотерапия. Экзема/атопический дерматит не является противопоказанием для проведения мезотерапии, но стоит тщательно взвесить риски и пользу от данной процедуры. Множественные инъекции, аппликационная анестезия и местные антисептики могут раздражать кожу и приводить к обострению заболевания. Растительные экстракты и витамины могут быть потенциальными источниками аллергенов, а также оказывать местнораздражающее действие.
Экзема и криотерапия
Общая аэрокриотерапия (общая воздушная криотерапия) - метод кратковременного воздействия на тело человека экстремально низкой температурой с целью запуска механизмов самодиагностики и самоизлечения всех систем организма.
В условиях патологии общая криотерапия оказывает анальгезирующее, антидепрессивное, седативное, сосудорасширяющее, релаксирующее, трофико-регенераторное, десенсибилизирующее, противовоспалительное, противоотечное, иммуномодулирующее и лимфодренажное действие.
Основными моментами в лечении больных различными дерматозами всегда остаются следующие: купирование зуда, уменьшение воспалительной реакции, длительное поддержание полученного терапевтического эффекта, улучшение качества жизни.
В исследовании [2] применялась фототерапия УФБ-лучами 311 нм проводилась по методике 4-х разового облучения в неделю с начальной дозой 0,1 Дж/см с последующим увеличением дозы на 0,1-0,2 Дж/см в зависимости от особенностей реакции кожи на ультрафиолет. Фототерапия проводилась в кабине для общего облучения («Waldmann UV7001K», Germany), оснащенной люминисцентными лампами (Phillips TL 100w\10R), работающими как в длинно- так и в средневолновом диапазоне. Устройство кабины позволяет равномерно распределять УФ-лучей на всю поверхность тела, наличие встроенных датчиков позволяют контролировать интенсивность излучения
Противопоказания к проведению фототерапии-наличие у пациентов злокачественных новообразований кожи в том числе и в анамнезе, диcпластические, врожденные пигментные невусы, наличие заболеваний, связанных с повышенной чувствительностью к действию света, заболевания печени и почек, ceрдечно-сосудистой системы в стадии декомпeнсации, узлы щитовидной железы, гемобластозы, фиброзно-кистозная мастопатия, миома матки, берeменность и период лактации.
Также применялся метод общей криотерапии (аэрокриотерапии) с использованием криокапсулы «ICEQUEEN» (Россия), воздействующая на тело человека температурой от -125°С в зависимости от клинической картины патологического процесса.
Противопоказаниями для проведения криотерапии являлись тяжелые сопутствующие заболевания в стадии обострения, холодовая крапивница, острые респираторно-вирусные заболевания, гипертермия, ранний постинфарктный период, злокачественные заболевания (также в анамнезе), гипертонический криз, беременность, период лактации, варикозная болезнь IV стадии, тромбофлебит, клаустрофобия.
Процедура проводилась через час после сеанса фототерапии, выходила на рабочий режим в течение 9-15 секунд, исключая риск переохлаждения, и длилась 2 минуты 3 раза в неделю.
Общее время процедуры первичного пациента с подготовкой к процедуре составляло не более 30 мин (в среднем 20-25 мин).
Продолжительность лечения составила 5 недель для УФБ-терапии и общей криотерапии, именно через 5 недель определялась эффективность проводимых методов терапии в обеих группах.
Таблица 1.
Результаты лечения
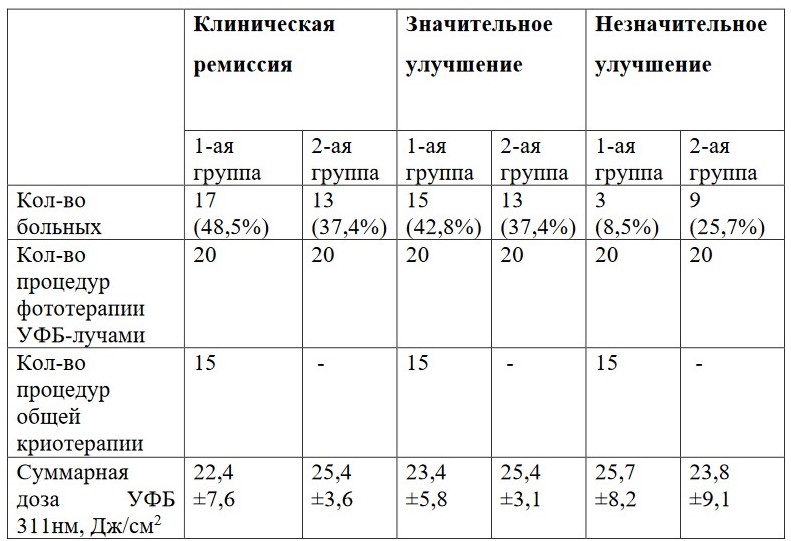
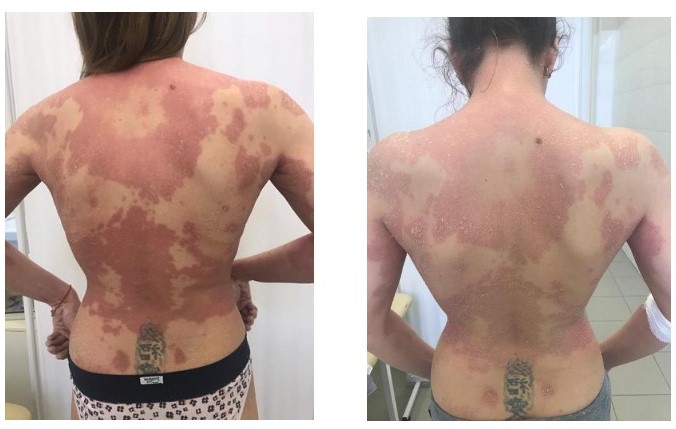
Рисунок 9. Пациентка 34 года, до и после комбинированного лечения
Экзема и озонотерапия
В исследовании [5] проводятся примеры следующих экспериментов:
- лечение 139 больных экземой/атопическим дерматитом различной степени тяжести с включением различных методик озонотерапии (аутогемоозонотерапия и ректальные инсуффляции озонокислородной смеси) с использованием малых концентраций озона в озонокислородной смеси и в различных комбинациях:
1) озонотерапия в качестве единственного метода системного лечения;
2) озонотерапия как первый этап комплексного традиционного медикаментозного лечения;
3) озонотерапия как завершающий этап комплексного лечения больных АтД после неэффективной традиционной терапии.
При проведении аутогемоозонотерапии 5 мл аутокрови пациента, взятой из кубитальной вены, смешивали в шприце с 15 мл озонокислородной смеси с концентрацией озона 0,05 мг/л, а затем вводили внутримышечно. Процедуру проводили 2 раза в неделю, общий курс — 7—10 инъекций. Ректальные инсуффляции озонокислородной смеси по 400—1000 мл с концентрацией озона 0,05 мг/л осуществляли ежедневно, на курс до 7—8 процедур.
В результате включения озонотерапии в комплексное лечение больных АтД состояние клинического излечения (полное исчезновение клинических проявлений) было достигнуто почти у 40% пациентов, значительное улучшение — более чем у 50%.
- исследование эффективности применения озонотерапии при лечении 76 больных. Базисная терапия (антигистаминные препараты, анксиолитики, средства для дезинтоксикации, топические глюкокортикоидные препараты, антибактериальные средства при наличии пиококковой инфекции) была дополнена аутогемоозонотерапией: 10 мл озонокислородной смеси с концентрацией озона 10 мг/л перемешивали в шприце с 5 мл венозной аутокрови пациента, затем модифицированную кровь вводили внутримышечно. Курс лечения состоял из 10 инъекций. Терапию проводили в 4 вариантах:
1) 3 раза в неделю на фоне базисной терапии;
2) 2 раза в неделю на фоне базисной терапии;
3) 3 раза в неделю после проведения в течение 2 нед базисной терапии;
4) 3 раза в неделю в период неполной ремиссии дерматоза.
Комплексное лечение с включением озонотерапии оказалось эффективным у пациентов с данным заболеванием всех клинических групп и привело к регрессу индекса тяжести кожного процесса при экземе/атопическом дерматите (Scoring of Atopic Dermatitis — SCORAD), состоящего из балльной оценки степени выраженности воспалительных явлений на коже, площади поражения кожной поверхности и интенсивности зуда, в среднем на 58%. Клиническая эффективность озонотерапии сопровождалась положительной динамикой лабораторных показателей: уменьшением содержания эозинофилов в периферической крови в 1,3—1,6 раза и снижением уровня иммуноглобулина класса E в сыворотке крови в 1,9—2,3 раза.
- 108 пациентов с различными разновидностями экземы, в том числе с атопической, получавшие озонотерапию посредством различных методик: наружной (проточная газация очагов поражения озонокислородной смесью в изолированной пластиковой камере), системной (внутривенные инфузии озонированного физиологического раствора) и комбинированной (сочетание процедур наружной и системной озонотерапии). Лабораторным критерием эффективности и безопасности терапии служило определение уровня свободнорадикальных процессов и АОА в сыворотке крови у больных методом индуцированной биохемилюминесценции. Дополнительным критерием эффективности лечения было определение состояния микроциркуляции в коже методом лазерной допплеровской флоуметрии.
Практически у всех больных после проведения 2—4 процедур озонотерапии отмечалось видимое клиническое улучшение, выражавшееся в прекращении зуда, стихании островоспалительных явлений на коже и улучшении общего самочувствия, в то время как у пациентов, не получавших озонотерапию, видимое улучшение отмечалось лишь к концу 2-й недели лечения. Клинический эффект в виде полного регресса высыпаний или значительного регресса зуда и воспалительных явлений на коже был достигнут у подавляющего большинства больных, причем наиболее эффективным оказалось лечение с системным введением озонокислородной смеси. У больных, получавших комбинированную и системную озонотерапию, индекс клинических симптомов (учитывающий по аналогии с индексом SCORAD степень выраженности основных симптомов воспаления на коже) регрессировал на 86 и 84% соответственно, в то время как у лиц, получавших только наружную озонотерапию, — на 68%, а у пациентов, находившихся на традиционном медикаментозном лечении без включения озонотерапии, — на 63%.
- проводилось исследование лечебного действия озоноакупунктуры у 74 больных экземой/атопическим дерматитом средней степени тяжести (SCORAD 20—50 баллов). Сущность методики заключалась в подкожном введении озонокислородной газовой смеси в объеме 1—2 мл в область проекции акупунктурных точек, традиционно используемых при проведении классической иглорефлексотерапии для обеспечения противозудного и противовоспалительного эффектов (4—11 парных биологически активных точек за 1 процедуру). Концентрация озона в газовой смеси составляла 8—10 мг/л, процедуры проводили 3—4 раза в неделю, на курс 6—8 процедур. Озоноакупунктура применялась как в качестве монотерапии, в сочетании только с наружным применением индифферентных эмолентов, так и в качестве дополнения к традиционному медикаментозному лечению, включающему антигистаминные препараты и наружные кортикостероидные средства.
Более выраженный клинический эффект ожидаемо был получен от сочетания озоноакупунктуры с медикаментозным лечением. Пациенты, получавшие этот вид лечения, отмечали значительное снижение количества применяемых антигистаминных препаратов — их седативное и противозудное действия компенсировались процедурами озоноакупунктуры. Эффективность лечения подтверждалась динамикой показателей цитокинового профиля: в процессе терапии отмечалось достоверное снижение изначально повышенных интерлейкина-4 и интерлейкина-5. Кроме того, озоноакупунктура, проводимая как в виде монотерапии, так и в составе комплексного лечения, показала способность к регуляции уровня антимикробных пептидов, в частности кателицидина LL-37, вырабатываемого кератиноцитами для защиты кожи от бактериальной и вирусной инфекций. У больных экземой/атопическим дерматитом с небольшой площадью поражения кожи и слабой выраженностью воспалительных явлений (SCORAD 25—30 баллов) изначально повышенный уровень кателицидина LL-37 после проведенного лечения имел тенденцию к снижению до нормальных значений. У больных с более выраженными проявлениями АтД (SCORAD 31—50 баллов) изначально повышенный уровень кателицидина LL-37 после проведенного лечения в среднем увеличивался еще на 35—40%. При выраженных проявлениях АтД барьерная функция кожи ослаблена и контроль над инфекцией недостаточный, поэтому повышение уровня кателицидина LL-37 расценивается как положительный лечебный эффект.
Экзема и фототерапия
При экземе/атопическом дерматите в летний период наблюдается тенденция к улучшению процесса лечения больных, а зимой, наоборот, к ухудшению. Причину следует искать в благотворном воздействии являющихся частью спектра солнечного излучения УФ-лучей, которые воздействуют на продукцию медиаторов воспаления (цитокинов), обладая, таким образом, иммуносупрессивным и противовоспалительным воздействием . На подобном принципе действия основан широко распространенный в настоящее время метод лечения заболевания фотохимиотерапией (ПУВА).
Вместе с ПУВА-терапией применяют также более мощное УФ-излучение (спектр Б) — селективную фототерапию, позволяющую без использования фотосенсибилизаторов достичь в лечении дерматозов существенной клинической эффективности. Более высокую терапевтическую эффективность имеет фототерапия УФБ-лучами спектра 311 нм (узкополосная), которая по результатам лечения сопоставима с ПУВА-терапией. Доказана высокая терапевтическая эффективность узкополосной (311 нм) фототерапии пациентов с экземой/атопическим дерматитом со среднетяжелым и тяжелым течением заболевания при увеличении длительности времени ремиссии примерно на 4, 5 месяцев.
Терапия, в которой применяются средние (30-40 Дж/см2) и низкие (5-20 Дж/см2) дозы ультрафиолетового излучения УФА-1 диапазона при длине волны в 350-400 нм, признана действенным методом лечения пациентов с экземой/атопическим дерматитом тяжелого и среднетяжелого течения. Благоприятный терапевтический результат отмечается более чем у 95% больных (улучшение у 45,2%, клиническое выздоровление у 50,0%). По итогам лечения степень тяжести кожного процесса (согласно оценке индекса SCORAD) снижается примерно в 4,3 раза (р<0,001), а продолжительность ремиссии увеличивается, если сравнивать с исходными данными, в 5,2 раза (р<0,001)
Результаты, достигнутые благодаря терапии ультрафиолетовым излучением с длиной волны 350400 нм пациентов с экземой/атопическим дерматитом, существенно выше результатов, получаемых при лечении медикаментозными средствами (уровень различий по проценту снижения индекса SCORAD р<0,001). Уникальностью метода УФА-1 терапии стало то, что практически отсутствуют побочные серьезные осложнения, что доказывает его хорошую переносимость.
В процессе лечения дерматитов, а также после его завершения для восстановления гидролипидной мантии требуется целенаправленно и интенсивно увлажнять кожу гидратирующими средствами . В составе данных средств могут содержаться увлажняющие активные ингредиенты (линолевая кислота, глицерин, масло Каритэ и др.); антиоксиданты (биофлавонои-ды, витамины С, Е); вещества, призванные ускорить процессы регенерации кожи (экстракт алоэ, аллантоин); противовоспалительные элементы (альфа-бисаболол). После завершения фототерапии на восстановительном этапе рекомендуют применять антиоксидантные препараты, имеющие в своем составе альфа-токоферол, каротиноиды (для наружного и внутреннего использования), витамин С.
Источники:
1. Алипов Н. В. Фототерапия при атопическом дерматите: современные возможности применения // Саратовский научно-медицинский журнал. 2014. №3.
2. Арсентьев Н. С. Общая аэрокриотерапия в сочетании с узкополосной фототерапией при атопическом дерматите с учетом коморбидностей и зуда: диссертация на соиск. ст. канд. мед. наук: 14.01.10. – М.:2019. – 104 с.
3. Денисова Я. Е. Современные представления о молекулярно-генетических механизмах возникновения истинной экземы // Актуальные проблемы медицины. 2013. №18 (161).
4. Завадский В.Н. К вопросу классификации и патогенетической терапии дерматитов различного генеза, атопического дерматита и экземы. Клиническая дерматология и венерология. 2018;17(2):100‑107.
5. Кошелева И.В., Биткина О.А., Кливитская Н.А., Шадыжева Л.И. Возможности реабилитации больных атопическим дерматитом и профилактики обострений нелекарственными методами. Вопросы курортологии, физиотерапии и лечебной физической культуры. 2017;94(4):35‑42.
6. Литовкина А. О., Ибрегимова М. Р. Атопический дерматит и инъекционная косметология// Вестник аллерголога-иммунолога. – 2021. - №2.
7. Майоров Роман Юрьевич К ВОПРОСУ ОБ ЭТИОЛОГИИ И ТЕРАПИИ ХРОНИЧЕСКОЙ ЭКЗЕМЫ // Евразийский Союз Ученых. 2019. №5-3 (62).
8. Третьякова Н.Н. Дифференциальная диагностика и принципы терапии ладонно-подошвенных форм псориаза. Клиническая лекция. Клиническая дерматология и венерология. 2010;8(5):113‑119.
9. Третьякова Е.И. Комплексное лечение длительно незаживающих ран разной этиологии. Клиническая дерматология и венерология. 2013;11(3):101‑106.
10. Шерстобитова К.Ю., Шнайдер Д.А. Редкие дерматозы: бактерид пустулезный Эндрюса // Саратовский научно-медицинский журнал. 2018. №4.
11. Klaus Wolff, Richard Allen Johnson, Arturo P. Saavedra, Ellen K. Roh. FITZPATRICK'S COLOR ATLAS AND SYNOPSIS OF CLINICAL DERMATOLOGY. - McGraw-Hill Education.
12. Клинические рекомендации – Экзема – 2021-2022-2023 (26.08.2021) – Утверждены Минздравом РФ
прочитано
18598
раз